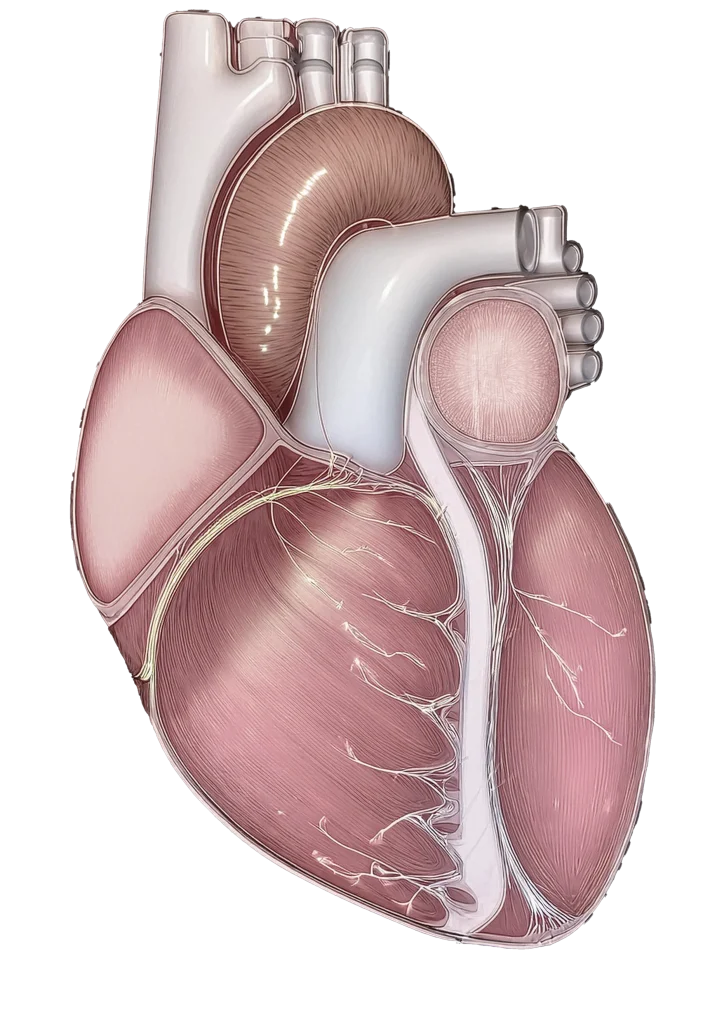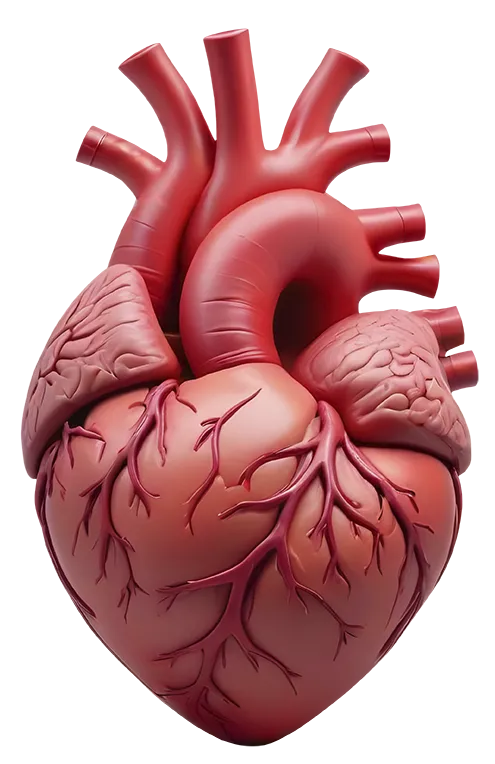
El infarto agudo de miocardio (IAM), provoca isquemia aguda y pérdida de tejido miocárdico, que progresa frecuentemente a IC crónica, debido a la baja respuesta regenerativa del corazónhumano. Además, la disfunción o la pérdida progresiva de cardiomiocitos (CMs) provocada por la hipertensión, el síndrome metabólico y el envejecimiento, también pueden provocar IC no isquémica, lo que supone un peso sociosanitario cada vez mayor. Nuevas terapias destinadas a regenerar el miocardio han sido objeto reciente de una intensa investigación básica y clínica, desafortunadamente con resultados no satisfactorios. Los intentos de obtener nuevos CMs a partir de células madre cardíacas no han tenido éxito hasta ahora, mientras que el uso de CMs derivados de células madre pluripotentes es problemático debido a la alogenia y las propiedades proarrítmogénicas de las células implantadas.
A diferencia del miocardio, el músculo esquelético contiene células madre llamadas células satélite (CSs), que pueden regenerar el músculo lesionado. Resultados anteriores han demostrado que las CSs del músculo de la mandíbula, pero no las CSs de otros músculos esqueléticos, pueden redirigirse in vitro a hacia CMs al exponerlos a un entorno de señalización cardiogénico.
Este proyecto evaluará si las CSs de los músculos masticatorios sepueden redirigir eficientemente hacia CMs funcionales mediante la combinación de enfoques in vitro, incluyendo la modulación de la vía de hipoxia y el control de la actividad de la telomerasa, así como el uso de biomateriales que imitan la matriz extracelular (ECM) y el entorno de señalización cardiogénico.
Además, exploraremos la relevancia traslacional de esta aproximación mediante el trasplante de los CMs derivados de CSs aislados o integrados en tejidos cardiacos creados mediante bioingeniería (EHTs) en corazones de ratón infartados.